Untersuchung Mesilat- und Besilat-haltiger Fertigarzneimittel auf potenziell genotoxische Verunreinigungen – Untersuchungsergebnisse 2009
Im Rahmen des Probenplans 2009 forderte das LGL Arzneispezialitäten bayerischer pharmazeutischer Unternehmer (PU) zur Untersuchung an, deren Wirkstoffe als Salze der Benzolsulfonsäure beziehungsweise Methansulfonsäure (vgl. Abb. 1) vorliegen. Ziel dieser Untersuchungen war es, im Sinne eines vorausschauenden Gesundheitsschutzes Arzneimittel auf diese genotoxischen Verunreinigungen zu analysieren. Dabei handelt es sich um Verunreinigungen, die durch Interaktion mit dem Erbgut möglicherweise Änderungen beziehungsweise Mutationen von Zellen auslösen und damit auch kanzerogen sein können.
Hintergrund
Sulfonsäuren kommen häufig im Verlauf von Wirkstoffsynthesen zum Einsatz, zum Beispiel als Gegenionen, als saure Katalysatoren oder auch als Schutzgruppen. In den verschiedenen Synthesestufen beziehungsweise während des Salzkristallisationsprozesses können Benzol- beziehungsweise Methansulfonsäure unter Anwesenheit eines niederkettigen Alkohols Sulfonsäureester bilden, die nachweislich DNA-alkylierende Eigenschaften besitzen und als potenziell genotoxisch einzustufen sind.
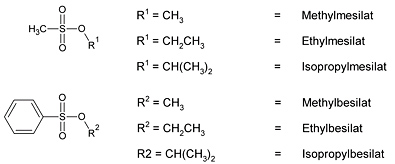
Abbildung 1: Chemische Struktur verschiedener Besilate und Mesilate
Die Anforderung, genotoxische Verunreinigungen grundsätzlich mit in die Qualitätskontrollen von Arzneimitteln einfließen zu lassen, fand im Jahr 2006 Eingang in die offiziellen Richtlinien der Europäischen Arzneibuch-Kommission. Mit der „Guideline on the Limits of Genotoxic Impurities" wurde von der European Medicines Agency (EMA) ein offizieller Grenzwert festgelegt (TTC = threshold of toxicological concern). Dieser setzt die tägliche Aufnahme von genotoxischen Verunreinigungen wie beispielsweise die erwähnten Sulfonsäureester auf maximal 1,5 µg/Person/Tag fest.
Um eine mögliche Gesundheitsgefährdung beurteilen zu können, muss zunächst geprüft werden, welches Gefährdungspotenzial tatsächlich von der spezifischen Verunreinigung ausgeht. Somit ist beispielsweise zu berücksichtigen, ob ein Arzneimittel nur für eine kurze Dauer (z. B. Antibiotika) oder langfristig bis lebenslang (z. B. Antihypertonika) eingenommen werden muss. In diesen Fällen kann der TTC gestaffelte Werte von 1,5 µg/Tag (Exposition > 12 Monate) bis 120 µg/Tag (Exposition = 1 Monat) annehmen.
Untersuchungen auf genotoxische Verunreinigungen
2009 untersuchte das LGL 57 Proben auf potenziell genotoxische Verunreinigungen. Bei der Untersuchung auf Benzolsulfonsäureester (Methyl-, Ethyl- und Isopropylbesilat) durch LC/MS-Verfahren konnten keinerlei bedenklich hohe Werte ermittelt werden. Lediglich bei zwei Proben waren Maximalwerte von annähernd 1 µg/Tag festzustellen. Die Bestimmung der Methansulfonsäureester (Methyl-, Ethyl- und Isopropylmesilat) mittels GC/MS zeigte, dass die Proben in der Regel den Anforderungen der EMA-Guideline entsprechen. Bei zwei Proben wurde der Grenzwert leicht, bei einer Probe mit bis zu 20,8 µg/Tag deutlich überschritten. Bei weiteren im Jahr 2011 gemessenen Proben konnten keine erhöhten Gehalte genotoxischer Verunreinigungen mehr festgestellt werden.
Fazit
Trotz der in diesem Fall überwiegend positiven Ergebnisse der Untersuchung sollten Hersteller verstärkt auf die Analytik genotoxischer Verunreinigungen und die Einhaltung der EMAGuideline achten. Dies umso mehr, als die Detektion derartiger Verunreinigungen häufig nicht mehr durch gängige Analysemethoden wie HPLC-UV gewährleistet werden kann, sondern modernerer Verfahren wie GC/MS oder LC/MS bedarf. Es zeigte sich darüber hinaus, dass die in Prüfvorschriften der Hersteller verankerten Nachweismethoden nicht immer dem wissenschaftlichen Stand entsprechen und nachgebessert werden müssten. Aus diesem Anlass erarbeitet die europäische Arzneibuch-Kommission EDQM drei allgemeine Monographien zur Bestimmung von Sulfonsäureestern in Arzneimitteln. Das LGL ist an der Entstehung der Vorschriften mit fachlicher Expertise beteiligt.
Wissenschaftliche Veröffentlichungen
- Wollein U, Schramek N. Simultaneous determination of alkyl mesilates and alkylbesilates in finished drug products by direct injection GC/MS. Eur J Pharm Sci 2012; 45(1-2): 201-204.
- Wollein U, Schramek N. Bestimmung von Alkylsulfonsäureestern in Mesilat- bzw. Besilatsalz-haltigen Arzneimitteln mittels GC/MS bzw. LC/MS. Pharm Ind 2011; 73: 574–580.

